Малокровие селезенки судебная медицина причины
Обновлено: 17.04.2024
Кафедра судебной медицины Военно-медицинской академии им. С.М. Кирова, Санкт-Петербург
Кафедра судебной медицины Военно-медицинской академии им. С.М. Кирова Минобороны России, Санкт-Петербург
Кафедра судебной медицины Военно-медицинской академии им. С.М. Кирова, Санкт-Петербург
Бюро судебно-медицинской экспертизы Ленинградской области
Бюро судебно-медицинской экспертизы Ленинградской области, Санкт-Петербург, Россия, 198095
Инфаркт или травматический разрыв селезенки?
Журнал: Судебно-медицинская экспертиза. 2017;60(3): 39‑41
Кафедра судебной медицины Военно-медицинской академии им. С.М. Кирова, Санкт-Петербург
Приведенный случай представляет интерес для судебно-медицинских экспертов в виду редкой встречаемости инфарктов селезенки в судебно-медицинской практике. Необходимы накопления информации о подобных случаях, тщательное изучение их и обобщение дифференциально-диагностических признаков травмы (разрыв селезенки) и патологии (инфаркта органа).
Кафедра судебной медицины Военно-медицинской академии им. С.М. Кирова, Санкт-Петербург
Кафедра судебной медицины Военно-медицинской академии им. С.М. Кирова Минобороны России, Санкт-Петербург
Кафедра судебной медицины Военно-медицинской академии им. С.М. Кирова, Санкт-Петербург
Бюро судебно-медицинской экспертизы Ленинградской области
Бюро судебно-медицинской экспертизы Ленинградской области, Санкт-Петербург, Россия, 198095
Как известно, инфаркт селезенки — это омертвение участка ткани органа, обусловленное острым локальным нарушением кровоснабжения [1]. В судебно-медицинской практике случаи инфаркта селезенки относятся к редким. Это обстоятельство ограничивает возможности экспертов в приобретении личного опыта достоверной дифференциальной диагностики данного вида патологии от закрытой травмы живота, проявившейся разрывом селезенки.
Приводим наблюдение из собственной практики.
02.01.12 в период с 18 до 20 ч пострадавший гр-н З., 36 лет, подвергся избиению. Удары наносились руками и ногами по голове, груди (по нижним ребрам слева) и животу. 10 января госпитализирован в нейрохирургическое отделение городской больницы по поводу закрытой черепно-мозговой травмы, сотрясения головного мозга, перелома правой скуловой кости и ушибом грудной клетки. При поступлении: живот напряжен, болезненный. Резкая болезненность при поколачивании по поясничной области слева и справа. Рентгенологическое исследование переломов ребер не выявлено. При ультразвуковом исследовании внутренних органов обнаружили увеличение левой доли печени до 95 мм (норма 60—90 мм), правой до 164 мм (норма 100—150 мм); селезенка размером 144×69 мм (норма 120×60). Структура органов однородная, контуры ровные. Под правой долей печени справа около 200 мл свободной жидкости. Заключение: гепатоспленомегалия, малый асцит. 12 января беспокоили боли в груди, болезненность в проекции нижних ребер слева. Живот мягкий, безболезненный. 13 января «за нарушение режима» (самовольно ушел из стационара) выписан «в удовлетворительном состоянии». Заключительный клинический диагноз: закрытая черепно-мозговая травма. Сотрясение головного мозга. Перелом правой скуловой кости. Ушиб грудной клетки.
31января после переохлаждения у гр-на З. появился сухой кашель, повысилась температура тела, при глубоком вдохе и кашле больной ощущал боли в левой половине груди, которые беспокоили и ранее, в период с 10 по 13 января. При физической нагрузке отмечал одышку, по-прежнему сохранялась повышенная температура тела, самостоятельно принимал баралгин как болеутоляющее и жаропонижающее средство. За медицинской помощью не обращался.
При амбулаторном врачебном осмотре 11 февраля гр-н З. жаловался на отсутствие стула в течение 6 дней. Объективно: общее состояние удовлетворительное, тоны сердца ритмичные, пульс 80 ударов в минуту. Артериальное давление 90/60 мм рт.ст. В нижних отделах левого легкого дыхание ослаблено, хрипов нет. Частота дыхательных движений 20 в минуту. Живот умеренно вздут, безболезненный. Общий анализ крови: гемоглобина 108 г/л, тромбоцитов 229·10 9 /л, лейкоцитов 13,5·10 9 /л, нейтрофилов: палочкоядерных 3%, сегментоядерных 78%, лимфоцитов 16%, моноцитов 3%, СОЭ 30 мм/ч. Общий анализ мочи: белок отсутствует, лейкоцитов 3—6 в поле зрения, диастаза 64 ед. 15 февраля гр-на З. беспокоили боли в левом подреберье с иррадиацией в левую поясную область; отсутствовал самостоятельный стул. Температура тела 38 °С в течение 8 дней. При рентгенологическом исследовании диагностирована острая левосторонняя полисегментарная пневмония, гидроторакс слева.
16 февраля госпитализирован в хирургическое отделение городской больницы, где находился на лечении по 3 марта. В день госпитализации беспокоили боли в нижних отделах груди, усиливающиеся при дыхании; одышка при физической нагрузке, общая слабость, отсутствие стула. Экстренной хирургической патологии не выявили.
17 февраля температура тела 38,5 °С. Тоны сердца ясные, ритмичные, шумов нет. Пульс 80—86 ударов в минуту. Артериальное давление 95/60 мм рт.ст. Частота дыхания 20 в минуту. Дыхание в легких везикулярное, с обеих сторон, ослаблено слева в нижних отделах, здесь же прослушиваются единичные влажные хрипы. Живот умеренно вздут, симметричен, мягкий, участвует в акте дыхания, при пальпации не напряжен, слегка болезненный в левом подреберье. Симптомов раздражения брюшины нет. Перистальтика кишечника активная. В связи с подозрением на наличие подкапсульного разрыва селезенки и реактивного плеврита слева, угрозы возникновения двухмоментного разрыва селезенки принято решение об оперативном вмешательстве по срочным показаниям.
Под общим наркозом проведены верхнесрединная лапаротомия, спленэктомия, санация и дренирование брюшной полости. При ревизии брюшной полости в левом подреберье прощупывался плотный конгломерат, состоящий из селезенки, селезеночного угла толстой кишки, желудка, сальника. После разрушения конгломерата вскрылся абсцесс объемом около 200 мл в виде слизеобразного гноя с детритом. Тупым путем выделили селезенку, представленную двумя равными частями. Одну часть органа удалось свободно удалить, другая держалась на сосудистой ножке. Селезенка была взята зажимом Федорова и отсечена, ее сосудистая ножка прошита. Гемостаз кровоточащих сосудов осуществляли путем прошивания капроном. Поддиафрагмальное пространство слева осушили, дренировали трубчатым и сигарообразным дренажем через прокол в левом подреберье. Операционную рану послойно ушили, наложили асептическую повязку.
Сведений об обнаружении крови или следов ее в свободной полости брюшины, повреждений связок селезенки в виде кровоизлияний, надрывов, кровоизлияний в мягких тканях груди и живота в проекции селезенки при клиническом обследовании пациента и интраоперационно в представленных медицинских документах не было. Диагноз: тупая травма живота, застарелый разрыв селезенки, поддиафрагмальный абсцесс слева.
При патоморфологическом исследовании удаленной селезенки установили, что она расчленена на два фрагмента. В одном из фрагментов имелся белый клиновидный очаг некроза с основанием размером 3×2 см, расположенным со стороны капсулы, а вершиной направленный к воротам органа (инфаркт). Паренхима селезенки малокровная, с диффузными кровоизлияниями, наличием дефекта, выполненного лизированной кровью, фибрином и гноем. Края разделения фрагментов селезенки вишневого цвета за счет пропитывания кровью.
При микроскопическом исследовании гистологических препаратов части селезенки с инфарктом выявили очаговый некроз паренхимы органа с множеством распавшихся гранулоцитов в центре очага, четкими клетками по периферии и наличием фибрина. Очаг инфаркта ограничен капсулой из рыхлой соединительной ткани, содержащей тонкие коллагеновые волокна, фибробласты, новообразованные сосуды умеренного кровенаполнения. Под капсулой — кровоизлияния из эритроцитов с размытыми контурами, наличием пигмента в небольшом количестве. По периферии очагов — фибробласты, лимфоциты. Красная пульпа малокровна. Капсула и подлежащий слой паренхимы селезенки некротизированы, по периферии — скопления выщелоченных эритроцитов, а вокруг очага некроза — разрушенные гранулоциты и новообразованная капсула из рыхлой соединительной ткани с полнокровными новообразованными сосудами с отложением бурого пигмента. В одном из полей зрения на удалении от капсулы определялся очаг некроза, окруженный выщелоченными эритроцитами, массы фибрина и его нити, участки врастания фибробластов, скопления четких гранулоцитов по периферии.
Выписан 03.03.12 в удовлетворительном состоянии в связи с самовольным уходом из стационара. До 25.03.12 находился на амбулаторном лечении у хирурга. Выписан к труду с 25.03.12.
В приведенном случае у гр-на З. подозревали разрыв селезенки как следствие избиения пострадавшего 02.01.12. До оперативного вмешательства (17.02) селезенка была заключена в единый плотный конгломерат, располагавшийся в левой поддиафрагмальной части полости брюшины, заключенный в спайки. После разрушения конгломерата в ходе операции селезенка была выделена в виде двух фрагментов. На период интраоперационного исследования гематомы селезенки не наблюдали, поскольку при разрушении конгломерата выделился гной с детритом (200 мл) ткани селезенки, а не кровь.
При сопоставлении медицинских данных и результатов повторного исследования гистологических препаратов селезенки гр-на З. с данными специальной литературы о диагностических признаках разрыва и инфаркта селезенки [1—7] экспертная комиссия установила, что в процессе клинических обследований гр-на З. объективных признаков, указывающих на наличие у пациента травматического разрыва селезенки, не выявлено.
При повторном экспертном исследовании материалов дела, в том числе и медицинских документов, судебно-гистологическом исследовании препаратов селезенки получены данные, достоверно указывающие на наличие у пострадавшего гр-на З. инфаркта селезенки, осложнившегося абсцессом селезенки и левосторонним осумкованным поддиафрагмальным абсцессом [3].
Это подтверждается характерной клиновидной формой очага некроза, белой окраской и ориентацией (основание очага со стороны капсулы с вершиной, направленной к воротам»), патологически измененным участком органа и результатами гистологического исследования препаратов селезенки.
Данный случай представляет несомненный интерес для судебно-медицинских экспертов в виду редкой встречаемости инфаркта селезенки в судебно-медицинской практике. Очевидно, требуется накопление информации о таких случаях с целью тщательного исследования и обобщения диагностических признаков, позволяющих проводить дифференциальную диагностику нетравматического первичного инфаркта селезенки от травматических разрывов и посттравматического инфаркта.
Нужна ваша помощь, делаю презентацию по механической асфиксии
Здравствуйте. Делаю презентацию по механической асфиксии, информация есть, а вот с фото напряг-в атласах и учебниках качество не очень,мягко говоря. В интернете того, что нужно не могу найти. Если у кого есть фото, таблицы или схемы - прошу поделиться. Заранее спасибо!
должна быть видна причина асфиксии. Например, если повешенье-борозда, удавление руками-следы от пальцев итд
и ещё появился вопрос - имеет место застойное венозное полнокровие всех внутренних органов, кроме селезенки.почему в ней нет застоя?? туплю, но понять не могу(
и ещё появился вопрос - имеет место застойное венозное полнокровие всех внутренних органов, кроме селезенки.почему в ней нет застоя?? туплю, но понять не могу(
". Своеобразно реагирует на асфиксический процесс селезенка. Впервые ее малокровие на фоне гиперемии других внутренних органов было отмечено 3. Ю. Сабинским (1865). Работа вызвала цикл проверочных исследований и длительную дискуссию среди судебных медиков, причем ряд авторов, например, П. В. Серебренников (1927), подвергли сомнению диагностическую значимость данного признака. Однако Д. П. Косоротов (1928), А. Д. Гусев (1938) вновь подтвердили судебно-медицинское значение анемии селезенки при диагностике странгуляций. Более того, А. Д. Гусев указал, что анемия и сокращение селезенки наиболее всего типичны для смерти от асфиксии, хотя и не постоянны. Причину сокращения этого органа автор видит в действии асфиксической крови на вазомоторы и сосуды, подчеркивая, что определенное значение в кровенаполнении играют прижизненные заболевания, например, малярия. А. И. Крат (1957, 1958) изучил состояние селезенки на трупном материале и в экспериментах на животных. Автор нашел в капсуле и трабекулах селезенки животных большое количество гладких мышечных волокон, отметив, что у человека их мало и преобладает густая сеть волокнистой соединительной ткани. Этим автор и объяснял преимущественное полнокровие органа, установленное им. В то же время В. И. Прозоровский (1968), А. С. Литвак (1970), описывая признаки смерти от странгуляционной асфиксии, Указывают анемию селезенки в их числе. Малокровие селезенки, наблюдаемое при повешении, может быть объяснено ее сокращением в результате рефлекторных воздействий с рецепторных зон шеи через блуждающие нервы (Крат А. И., 1958), непосредственным и через сосудодвигательные центры продолговатого мозга действием асфиксической крови на вазомоторы (Королько Л. Ф., 1975), влиянием дополнительного выброса в кровь катехоламинов (Чвалун А. В., 1976).
При экспериментальном повешении кроликов мы наблюдали малокровие селезенки в 46 случаях из 72, как правило, у тех животных, которые погибали очень быстро (полное повешение с рывком в затягивающейся петле). На экспертном материале этот признак отмечен нами в 63 % случаев. Следует отметить, что в настоящее время феномен сокращения селезенки при действии различных факторов наглядно подтвержден клиницистами при ультразвуковых исследованиях органов брюшной полости. Селезенка на вскрытии при смерти от повешения, как правило, небольшая, со сморщенной бледной капсулой, на разрезе серо-розовая или светло-красная, с зернистой пульпой и подчеркнутыми трабекулами, без значительного соскоба. В плане правильной оценки этого симптома следует иметь в виду легкость его исчезновения при аутолитических изменениях, возможность влияния фоновой патологии. Так, небольшая селезенка встречается при кахексии, серповидно-клеточной анемии, в позднем старческом возрасте. Атрофия селезенки при этих состояниях сопровождается возникновением фиброза, кальциноза, гемосидероза. Указанные патологические состояния при экспертизе повешения встречаются достаточно редко, что дает основание считать анемию селезенки достоверным общеасфиксическим признаком, а длившуюся более столетия дискуссию о практическом его значении законченной."
Осталось дело за малым, когда найдёте автора этих строк "тупить" уже не будете
". Своеобразно реагирует на асфиксический процесс селезенка. Впервые ее малокровие на фоне гиперемии других внутренних органов было отмечено 3. Ю. Сабинским (1865). Работа вызвала цикл проверочных исследований и длительную дискуссию среди судебных медиков, причем ряд авторов, например, П. В. Серебренников (1927), подвергли сомнению диагностическую значимость данного признака. Однако Д. П. Косоротов (1928), А. Д. Гусев (1938) вновь подтвердили судебно-медицинское значение анемии селезенки при диагностике странгуляций. Более того, А. Д. Гусев указал, что анемия и сокращение селезенки наиболее всего типичны для смерти от асфиксии, хотя и не постоянны. Причину сокращения этого органа автор видит в действии асфиксической крови на вазомоторы и сосуды, подчеркивая, что определенное значение в кровенаполнении играют прижизненные заболевания, например, малярия. А. И. Крат (1957, 1958) изучил состояние селезенки на трупном материале и в экспериментах на животных. Автор нашел в капсуле и трабекулах селезенки животных большое количество гладких мышечных волокон, отметив, что у человека их мало и преобладает густая сеть волокнистой соединительной ткани. Этим автор и объяснял преимущественное полнокровие органа, установленное им. В то же время В. И. Прозоровский (1968), А. С. Литвак (1970), описывая признаки смерти от странгуляционной асфиксии, Указывают анемию селезенки в их числе. Малокровие селезенки, наблюдаемое при повешении, может быть объяснено ее сокращением в результате рефлекторных воздействий с рецепторных зон шеи через блуждающие нервы (Крат А. И., 1958), непосредственным и через сосудодвигательные центры продолговатого мозга действием асфиксической крови на вазомоторы (Королько Л. Ф., 1975), влиянием дополнительного выброса в кровь катехоламинов (Чвалун А. В., 1976).
При экспериментальном повешении кроликов мы наблюдали малокровие селезенки в 46 случаях из 72, как правило, у тех животных, которые погибали очень быстро (полное повешение с рывком в затягивающейся петле). На экспертном материале этот признак отмечен нами в 63 % случаев. Следует отметить, что в настоящее время феномен сокращения селезенки при действии различных факторов наглядно подтвержден клиницистами при ультразвуковых исследованиях органов брюшной полости. Селезенка на вскрытии при смерти от повешения, как правило, небольшая, со сморщенной бледной капсулой, на разрезе серо-розовая или светло-красная, с зернистой пульпой и подчеркнутыми трабекулами, без значительного соскоба. В плане правильной оценки этого симптома следует иметь в виду легкость его исчезновения при аутолитических изменениях, возможность влияния фоновой патологии. Так, небольшая селезенка встречается при кахексии, серповидно-клеточной анемии, в позднем старческом возрасте. Атрофия селезенки при этих состояниях сопровождается возникновением фиброза, кальциноза, гемосидероза. Указанные патологические состояния при экспертизе повешения встречаются достаточно редко, что дает основание считать анемию селезенки достоверным общеасфиксическим признаком, а длившуюся более столетия дискуссию о практическом его значении законченной."
Осталось дело за малым, когда найдёте автора этих строк "тупить" уже не будете
Спленомегалия — вторичный патологический синдром, который проявляется увеличением размеров селезенки. Увеличение органа невоспалительного генеза сопровождается ноющей болью, чувством распирания в левом подреберье. При инфекционных процессах возникает лихорадка, резкая боль в подреберье слева, тошнота, диарея, рвота, слабость. Диагностика основывается на данных физикального осмотра, УЗИ, сцинтиграфии селезенки, обзорной рентгенографии и МСКТ брюшной полости. Тактика лечения зависит от основного заболевания, которое привело к спленомегалии. Назначают этиотропную терапию, при необратимых изменениях и значительном увеличении органа выполняют спленэктомию.
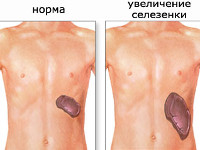

Общие сведения
Спленомегалия – аномальное увеличение селезенки. Синдром не является самостоятельной нозологической единицей, а возникает вторично, на фоне другого патологического процесса в организме. В норме селезенка весит около 100-150 г и не доступна для пальпации, т. к. полностью скрыта под реберным каркасом. Пальпаторно определить орган удается при его увеличении в 2-3 раза. Спленомегалия может являться индикатором серьезных болезней, ее распространённость в общей популяции составляет 1-2%. У 5-15% здоровых детей определяется гипертрофия селезенки ввиду несовершенства иммунной системы. Синдром может встречаться у людей всех возрастов. В равной степени поражает лиц женского и мужского пола.

Причины спленомегалии
Селезенка является важной составляющей иммунной системы. Повышение функциональной активности, увеличение скорости кровотока и размеров органа сопровождает большое количество заболеваний как инфекционной, так и неинфекционной природы. К основным причинам развития данной патологии относят:
- Инфекционные заболевания. Увеличение размеров происходит в результате повышенной иммунной нагрузки на орган при бактериальных (сифилис, туберкулез), вирусных (ВИЧ, цитомегаловирус, вирус Эпштейна–Барр), грибковых (бластомикоз, гистоплазмоз), паразитарных (шистосомоз, эхинококкоз), протозойных (малярия, лейшманиоз) острых и хронических инфекциях.
- Аутоиммунные заболевания. Гиперплазия развивается при повышении фагоцитарной функции селезенки, активации ретикулоэндотелиальной системы на фоне аутоиммунных болезней (ревматоидный артрит, системная красная волчанка, узелковый периартериит).
- Миелопролиферативные болезни. Спленомегалия формируется при злокачественной трансформации костномозговых клеток, что сопровождается их избыточной пролиферацией и нарушением гемопоэза в т. ч. в селезенке. К данным состояниям можно отнести истинную полицитемию, миелолейкоз, миелоидную метаплазию.
- Новообразования различной этиологии. Увеличение органа может быть связано с доброкачественными и злокачественными образованиями селезенки, опухолями кроветворной системы (лимфома, острый и хронический лейкоз) и с метастазированием из других очагов (рак легкого, рак печени).
- Гематологические расстройства. Синдром развивается на фоне повышения функциональной нагрузки на селезенку при наследственных и приобретенных заболеваниях крови (гемолитическая анемия, талассемия, циклический агранулоцитоз и др.).
- Нарушения обмена веществ. Спленомегалия возникает в результате инфильтрации паренхимы макрофагами, липидами или другими метаболитами при приобретённых и наследственных нарушениях обмена веществ (фенилкетонурия, болезнь Вильсона, синдром Зольвегера, гликогенозы и др.).
- Нарушение кровообращения. При нарушении оттока крови по венозному руслу в результате застойных явлений происходит рост сосудистой ткани, увеличивается число эритроцитов, повышается давление в портальной системе, развивается гипертрофия органа. К данному состоянию может привести тромбоз селезеночной вены, перекручивание сосудистой ножки селезенки.
Классификация
В гастроэнтерологии синдром классифицируется в зависимости от этиологии и патогенеза. Выделяют две формы спленомегалии, имеющие различную природу и клинические проявления:
- Воспалительная. Возникает на фоне бактериальной, вирусной, протозойной, грибковой инфекции (острый вирусный гепатит, краснуха, туберкулез, сальмонеллез, малярия и др.). Проявляется яркой клинической картиной и общей интоксикацией организма.
- Невоспалительная. Развивается в результате различных заболеваний неинфекционной природы (анемии, амилоидоз, цирроз печени, лейкозы). В данном случае более выраженными являются симптомы основного заболевания, клинические проявления со стороны селезенки носят стертый характер.
Симптомы спленомегалии
Клиническая картина зависит от исходной патологии, причин и степени увеличения органа. В большинстве случаев на первый план выходят симптомы первичного заболевания. Воспалительные спленомегалии сопровождаются повышением температуры тела до фебрильных значений, тошнотой, рвотой, послаблением стула, выраженной слабостью. Болезненные ощущения часто носят острый режущий характер и локализуются в области левого подреберья.
При невоспалительной этиологии заболевания температура тела нормальная или субфебрильная. Возникает тупая ноющая или давящая боль в левом подреберье слабой интенсивности. Общие симптомы интоксикации отсутствуют или слабо выражены. Синдром спленомегалии сопровождается появлением бледности кожных покровов с синеватым оттенком, снижением аппетита, уменьшением работоспособности. Часто отмечается одновременное увеличение размеров селезенки и печени - гепатоспленомегалия. В этом случае к основным симптомам присоединяется чувство тяжести и распирания в подреберье справа.
Осложнения
К наиболее серьезным осложнениям спленомегалии относится разрыв селезенки. Данное состояние сопровождается массивным кровотечением и приводит к развитию геморрагического шока, а при отсутствии экстренных мер - к летальному исходу. Нарушение функции селезенки может сочетаться с внутриорганным разрушением форменных элементов крови, возникновением гиперспленизма, который сопровождается лейкопенией, анемией, тромбоцитопенией. В результате нарушается свертываемость крови, снижается иммунная функция организма, развивается гипоксия. Данное состояние может привести к жизнеугрожающим последствием (шок, кровотечение).
Диагностика
Первичная диагностика заключается в консультации гастроэнтеролога. Во время физикального осмотра специалист пальпаторно определяет патологически увеличенный орган, перкуторно - изменённую селезеночную тупость. С помощью изучения анамнеза жизни и заболевания врач может предположить причину, повлекшую развитие спленомегалии. Для подтверждения диагноза и проведения дифференциальной диагностики назначают следующие инструментальные исследования:
- УЗИ селезёнки. Позволяет определить размеры и форму органа. Выявляет травмы, воспалительные процессы, новообразования и аномалии развития селезенки.
- Обзорная рентгенография брюшной полости. На снимках определяется увеличение селезенки и смещение близлежащих анатомических структур (желудка, кишечника). При рентгеноскопии селезенка подвижна и участвует в акте дыхания.
- МСКТ брюшной полости. Современный метод исследования, который позволяет получить детальное изображение органа. При локализации первичного заболевания в брюшной полости (опухоль, эхинококковая киста) данный способ помогает определить причину спленомегалии.
- Сцинтиграфия селезенки. С помощью радиоизотопного исследования можно определить функциональное состояние и очаговые изменения селезеночной паренхимы. Одновременно часто проводится сцинтиграфия печени, что может помочь в поиске причины болезни.

При ярко выраженной клинической картине с симптомами интоксикации назначают ОАК, биохимический анализ крови, ОАМ. Спленомегалию дифференцируют с доброкачественными и злокачественными образованиями, абсцессом, кистой селезенки.
Лечение спленомегалии
Тактика лечения основана на поиске и устранении причинного заболевания. При инфекционных процессах терапия проводится с учетом возбудителя болезни (антибактериальные, противовирусные, противопротозойные препараты и др.). При аутоиммунной патологии назначают гормональные средства. При гематологических заболеваниях и новообразованиях применяют противоопухолевые препараты, лучевую и химиотерапию, пересадку костного мозга. Воспалительные спленомегалии с выраженными симптомами интоксикации требуют проведения дезинтоксикационной, противовоспалительной терапии. Симптоматически назначают витамины и минеральные комплексы, обезболивающие препараты.
При больших размерах селезенки, некоторых болезнях накопления (амилоидоз, болезнь Гоше и др.), гиперспленизме, тромбозе воротной и селезеночной вен выполняют удаление органа (спленэктомию). Диета при спленомегалии предполагает отказ от жаренных, копченных, консервированных блюд, алкогольных напитков. Рекомендовано сократить употребление сдобной выпечки, грибов, кофе, шоколада, газированных напитков. Следует отдавать предпочтение нежирным сортам мяса (крольчатина, говядина), овощам (перец, капуста, свекла), крупам, фруктам и ягодам (цитрусовые, бананы, яблоки, малина и др.). Из напитков рекомендуется употреблять некрепкий чай, морсы и компоты собственного приготовления.
Прогноз и профилактика
Спленомегалия - синдром, который может свидетельствовать о серьезных заболеваниях и потому требует проведения тщательной диагностики. Дальнейшие перспективы зависят от первоначальной патологии. Прогнозирование последствий заболевания не представляется возможным из-за многофакторности данного состояния. Профилактика заключается в предупреждении развития патологии, которая приводит к формированию спленомегалии. С этой целью рекомендовано ежегодное диспансерное наблюдение, своевременное лечение острых процессов в организме и санация хронических очагов воспаления.
Гемолитическая анемия – патология эритроцитов, отличительным признаком которой является ускоренное разрушение красных кровяных телец с высвобождением повышенного количества непрямого билирубина. Для данной группы заболеваний типично сочетание анемического синдрома, желтухи и увеличения размеров селезенки. В процессе диагностики исследуется общий анализ крови, уровень билирубина, анализ кала и мочи, УЗИ органов брюшной полости; проводится биопсия костного мозга, иммунологические исследования. В качестве методов лечения используется медикаментозная, гемотрансфузионная терапия; при гиперспленизме показана спленэктомия.
МКБ-10
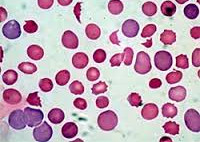


Общие сведения
Гемолитическая анемия (ГА) - малокровие, обусловленное нарушением жизненного цикла эритроцитов, а именно преобладанием процессов их разрушения (эритроцитолиза) над образованием и созреванием (эритропоэзом). Данная группа анемий очень обширна. Их распространенность неодинакова в различных географических широтах и возрастных когортах; в среднем патология встречается у 1% населения. Среди прочих видов анемий на долю гемолитических приходится 11%. Патология характеризуется укорочением жизненного цикла эритроцитов и их распадом (гемолизом) раньше времени (через 14-21 день вместо 100-120 суток в норме). При этом разрушение эритроцитов может происходить непосредственно в сосудистом русле (внутрисосудистый гемолиз) или в селезенке, печени, костном мозге (внесосудистый гемолиз).

Причины
Этиопатогенетическую основу наследственных гемолитических синдромов составляют генетические дефекты мембран эритроцитов, их ферментных систем либо структуры гемоглобина. Данные предпосылки обусловливают морфофункциональную неполноценность эритроцитов и их повышенное разрушение. Гемолиз эритроцитов при приобретенных анемиях наступает под влиянием внутренних факторов или факторов окружающей среды, среди которых:
- Аутоиммунные процессы. Образование антител, агглютинирующих эритроциты, возможно при гемобластозах (остром лейкозе, хроническом лимфолейкозе, лимфогранулематозе), аутоиммунной патологии (СКВ, неспецифическом язвенном колите), инфекционных заболеваниях (инфекционном мононуклеозе, токсоплазмозе, сифилисе, вирусной пневмонии). Развитию иммунных гемолитических анемий могут способствовать посттрансфузионные реакции, профилактическая вакцинация, гемолитическая болезнь плода.
- Токсическое действие на эритроциты. В ряде случаев острому внутрисосудистому гемолизу предшествует отравление мышьяковистыми соединениями, тяжелыми металлами, уксусной кислотой, грибными ядами, алкоголем и др. Вызывать разрушение клеток крови может прием определенных лекарств (противомалярийных препаратов, сульфаниламидов, производных нитрофуранового ряда, анальгетиков).
- Механическое повреждение эритроцитов. Гемолиз эритроцитов может наблюдаться при тяжелых физических нагрузках (длительной ходьбе, беге, лыжном переходе), при ДВС-синдроме, малярии, злокачественной артериальной гипертензии, протезировании клапанов сердца и сосудов, проведении гипербарической оксигенации, сепсисе, обширных ожогах. В этих случаях под действием тех или иных факторов происходит травматизация и разрыв мембран изначально полноценных эритроцитов.

Патогенез
Центральным звеном патогенеза ГА является повышенное разрушение эритроцитов в органах ретикулоэндотелиальной системы (селезенке, печени, костном мозге, лимфатических узлах) или непосредственно в сосудистом русле. При аутоиммунном механизме анемии происходит образование антиэритроцитарных АТ (тепловых, холодовых), которые вызывают ферментативный лизис мембраны эритроцитов. Токсические вещества, являясь сильнейшими окислителями, разрушают эритроцит за счет развития метаболических, функциональных и морфологических изменений оболочки и стромы красных кровяных телец. Механические факторы оказывают прямое воздействие на клеточную мембрану. Под влиянием этих механизмов из эритроцитов выходят ионы калия и фосфора, а внутрь поступают ионы натрия. Клетка разбухает, при критическом увеличении ее объема наступает гемолиз. Распад эритроцитов сопровождаются развитием анемического и желтушного синдромов (так называемой «бледной желтухой»). Возможно интенсивное окрашивание кала и мочи, увеличение селезенки и печени.
Классификация
В гематологии гемолитические анемии подразделяются на две большие группы: врожденные (наследственные) и приобретенные. Наследственные ГА включают следующие формы:
- эритроцитарные мембранопатии (микросфероцитоз – болезнь Минковского-Шоффара, овалоцитоз, акантоцитоз) – анемии, обусловлены структурными аномалиями мембран эритроцитов
- ферментопении (энзимопении) – анемии, вызванные дефицитом тех или иных ферментов (глюкозо-6-фосфатдегидрогеназы, пируваткиназы и др.)
- гемоглобинопатии- анемии, связанные с качественными нарушениями структуры гемоглобина или изменением соотношения его нормальных форм (талассемия, серповидно-клеточная анемия).
Приобретенные ГА подразделяются на:
- мембранопатии приобретенные (пароксизмальная ночная гемоглобинурия – б-нь Маркиафавы-Микели, шпороклеточная анемия)
- иммунные (ауто- и изоиммунные) – обусловлены воздействием антител
- токсические – анемии, обусловленные воздействием химических веществ, биологических ядов, бактериальных токсинов
- механические - анемии, вызванные механическим повреждением структуры эритроцитов (тромбоцитопеническая пурпура, маршевая гемоглобинурия)
Симптомы
Наследственные мембранопатии, ферментопении и гемоглобинопатии
Наиболее распространенной формой данной группы анемий является микросфероцитоз, или болезнь Минковского-Шоффара. Наследуется по аутосомно-доминантному типу; обычно прослеживается у нескольких представителей семьи. Дефектность эритроцитов обусловлена дефицитом в мембране актомиозиноподобного белка и липидов, что приводит к изменению формы и диаметра эритроцитов, их массивному и преждевременному гемолизу в селезенке. Манифестация микросфероцитарной ГА возможна в любом возрасте (в младенчестве, юношестве, старости), однако обычно проявления возникают у детей старшего возраста и подростков. Тяжесть заболевания варьирует от субклинического течения до тяжелых форм, характеризующихся часто повторяющимися гемолитическими кризами. В момент криза нарастает температура тела, головокружение, слабость; возникают боли в животе и рвота.
Основным признаком микросфероцитарной гемолитической анемии служит желтуха различной степени интенсивности. Вследствие высокого содержания стеркобилина кал становится интенсивно окрашенным в темно-коричневый цвет. У пациентов с болезнь Минковского-Шоффара наблюдается склонность к образованию камней в желчном пузыре, поэтому часто развиваются признаки обострения калькулезного холецистита, возникают приступы желчной колики, а при закупорке холедоха конкрементом - обтурационная желтуха. При микросфероцитозе во всех случаях увеличена селезенка, а у половины пациентов – еще и печень. Кроме наследственной микросфероцитарной анемии, у детей часто встречаются другие врожденные дисплазии: башенный череп, косоглазие, седловидная деформация носа, аномалии прикуса, готическое нёбо, полидактилия или брадидактилия и пр. Пациенты среднего и пожилого возраста страдают трофическими язвами голени, которые возникают в результате гемолиза эритроцитов в капиллярах конечностей и плохо поддаются лечению.
Энзимопенические анемии связаны с недостатком определенных ферментов эритроцитов (чаще - Г-6-ФД, глутатион-зависимых ферментов, пируваткиназы и др). Гемолитическая анемия может впервые заявлять о себе после перенесенного интеркуррентного заболевания или приема медикаментов (салицилатов, сульфаниламидов, нитрофуранов). Обычно заболевание имеет ровное течение; типична «бледная желтуха», умеренная гепатоспленомегалия, сердечные шумы. В тяжелых случаях развивается ярко выраженная картина гемолитического криза (слабость, рвота, одышка, сердцебиение, коллаптоидное состояние). В связи с внутрисосудистым гемолизом эритроцитов и выделением гемосидерина с мочой последняя приобретает темный (иногда черный) цвет. Особенностям клинического течения гемоглобинопатий - талассемии и серповидно-клеточной анемии посвящены самостоятельные обзоры.
Приобретенные гемолитические анемии
Среди различных приобретенных вариантов чаще других встречаются аутоиммунные анемии. Для них общим пусковым фактором выступает образование антител к антигенам собственных эритроцитов. Гемолиз эритроцитов может носить как внутрисосудистый, так и внутриклеточный характер. Гемолитический криз при аутоиммунной анемии развивается остро и внезапно. Он протекает с лихорадкой, резкой слабостью, головокружением, сердцебиением, одышкой, болями в эпигастрии и пояснице. Иногда острым проявлениям предшествуют предвестники в виде субфебрилитета и артралгий. В период криза стремительно нарастает желтуха, не сопровождающаяся кожным зудом, увеличивается печень и селезенка. При некоторых формах аутоиммунных анемий больные плохо переносят холод; в условиях низких температур у них может развиваться синдром Рейно, крапивница, гемоглобинурия. Вследствие недостаточности кровообращения в мелких сосудах возможны осложнения в виде гангрены пальцев ног и рук.
Токсические анемии протекают с прогрессирующей слабостью, болями в правом подреберье и поясничной области, рвотой, гемоглобинурией, высокой температурой тела. Со 2-3 суток присоединяется желтуха и билирубинемия; на 3-5 сутки возникает печеночная и почечная недостаточность, признаками которых служат гепатомегалия, ферментемия, азотемия, анурия. Отдельные виды приобретенных гемолитических анемий рассмотрены в соответствующих статьях: «Гемоглобинурия» и «Тромбоцитопеническая пурпура», «Гемолитическая болезнь плода».
Осложнения
Каждый вид ГА имеет свои специфические осложнения: например, ЖКБ – при микросфероцитозе, печеночная недостаточность – при токсических формах и т.д. К числу общих осложнений относятся гемолитические кризы, которые могут провоцироваться инфекциями, стрессами, родами у женщин. При остром массивном гемолизе возможно развитие гемолитической комы, характеризующейся коллапсом, спутанным сознанием, олигурией, усилением желтухи. Угрозу жизни больного несут ДВС-синдром, инфаркт селезенки или спонтанный разрыв органа. Неотложной медицинской помощи требуют острая сердечно-сосудистая и почечная недостаточность.
Диагностика
Определение формы ГА на основе анализа причин, симптоматики и объективных данных относится к компетенции гематолога. При первичной беседе выясняется семейный анамнез, частота и тяжесть протекания гемолитических кризов. В процессе осмотра оценивается окраска кожных покровов, склер и видимых слизистых, производится пальпация живота для оценки величины печени и селезенки. Сплено- и гепатомегалия подтверждается при проведении УЗИ печени и селезенки. Лабораторный диагностический комплекс включает:
- Исследование крови. Изменения в гемограмме характеризуются нормо- или гипохромной анемией, лейкопенией, тромбоцитопенией, ретикулоцитозом, ускорением СОЭ. В биохимических пробах крови определяется гипербилирубинемия (увеличение фракции непрямого билирубина), увеличение активности лактатдегидрогеназы. При аутоиммунных анемиях большое диагностическое значение имеет положительная проба Кумбса.
- Анализы мочи и кала. Исследование мочи выявляет протеинурию, уробилинурию, гемосидеринурию, гемоглобинурию. В копрограмме повышено содержание стеркобилина.
- Миелограмму. Для цитологического подтверждения выполняется стернальная пункция. Исследование пунктата костного мозга обнаруживает гиперплазию эритроидного ростка.
В процессе дифференциальной диагностики исключаются гепатиты, цирроз печени, портальная гипертензия, гепатолиенальный синдром, порфирии, гемобластозы. Пациента консультируют гастроэнтеролог, клинический фармаколог, инфекционист и другие специалисты.

Лечение
Различные формы ГА имеют свои особенности и подходы к лечению. При всех вариантах приобретенной гемолитической анемии необходимо позаботиться об устранении влияния гемолизирующих факторов. Во время гемолитических кризов больным необходимы инфузии растворов, плазмы крови; витаминотерапия, по необходимости – гормоно- и антибиотикотерапия. При микросфероцитозе единственно эффективным методом, приводящим к 100 % прекращению гемолиза, является спленэктомия.
При аутоиммунной анемии показана терапия глюкокортикоидными гормонами (преднизолоном), сокращающая или прекращающая гемолиз. В некоторых случаях требуемый эффект достигается назначением иммунодепрессантов (азатиоприна, 6-меркаптопурина, хлорамбуцила), противомалярийных препаратов (хлорохина). При резистентных к медикаментозной терапии формах аутоиммунной анемии выполняется спленэктомия. Лечение гемоглобинурии предполагает переливание отмытых эритроцитов, плазмозаменителей, назначение антикоагулянтов и антиагрегантов. Развитие токсической гемолитической анемии диктует необходимость проведения интенсивной терапии: дезинтоксикации, форсированного диуреза, гемодиализа, по показаниям – введение антидотов.
Прогноз и профилактика
Течение и исход зависят от вида анемии, тяжести протекания кризов, полноты патогенетической терапии. При многих приобретенных вариантах устранение причин и полноценное лечение приводит к полному выздоровлению. Излечения врожденных анемий добиться нельзя, однако возможно достижение длительной ремиссии. При развитии почечной недостаточности и других фатальных осложнений прогноз неблагоприятен. Предупредить развитие ГА позволяет профилактика острых инфекционных заболеваний, интоксикаций, отравлений. Запрещается бесконтрольное самостоятельное использование лекарственных препаратов. Необходимо тщательная подготовка пациентов к гемотрансфузиям, вакцинации с проведением всего комплекса необходимых обследований.
4. Клинические рекомендации по диагностике и лечению аутоиммунных гемолитический анемий/ Цветаева Н.В., Никулина О.Ф. - 2014.
Разрыв селезенки – это нарушение целостности селезенки в результате травматического воздействия. Возникает при ударе в нижнюю часть левой половины грудной клетки или в область левого подреберья. Часто сочетается с повреждением других органов брюшной полости. Проявляется болями в левом подреберье и симптомами кровопотери, обычно наблюдаются признаки раздражения брюшины. Диагноз выставляется на основании клинических проявлений, данных лапароскопии и других исследований. Лечение оперативное - ушивание селезенки или удаление органа.
МКБ-10


Общие сведения
Разрыв селезенки – достаточно распространенное повреждение. Из-за высокой вероятности обильного кровотечения представляет непосредственную опасность для жизни, требует проведения немедленного оперативного вмешательства. Чаще встречается у лиц трудоспособного возраста, что обусловлено их более высокой физической активностью и более высоким риском попадания в экстремальные ситуации.
Разрывы селезенки могут быть изолированными, встречаться в составе сочетанной и множественной травмы (политравмы). Часто наблюдаются одновременные повреждения печени, брыжейки и толстой кишки. Возможно сочетание с переломами ребер, повреждением грудной клетки, переломом позвоночника, ЧМТ, переломом таза, переломами костей конечностей и другими повреждениями. Лечение данной патологии осуществляют травматологи и абдоминальные хирурги.

Причины
Разрыв селезенки встречается при различных высокоэнергетических травмах: падениях с высоты, промышленных, природных, железнодорожных или автодорожных катастрофах. К числу предрасполагающих факторов, повышающих вероятность повреждения селезенки, относятся недостаточно прочная тонкая капсула, полнокровие органа и его малая подвижность. С другой стороны, эти факторы нивелируются тем, что селезенка достаточно надежно защищена от внешних воздействий ребрами. Вероятность разрыва селезенки в результате травмы увеличивается при патологических процессах, сопровождающихся спленомегалией и повышением рыхлости паренхимы. Кроме того, прочность селезенки в некоторой степени зависит от степени ее кровенаполнения, положения органа в момент травмы, фазы дыхания, наполнения кишечника и желудка.
Патанатомия
Селезенка – паренхиматозный орган, расположенный в верхней левой части брюшной полости, кзади от желудка, на уровне IX-XI ребер. Покрыта капсулой. Имеет форму удлиненной и уплощенной полусферы, которая выпуклой стороной обращена к диафрагме, а вогнутой – к органам брюшной полости. Селезенка не относится к числу жизненно важных органов. Является основным источником лимфоцитов, продуцирует антитела, участвует в разрушении старых тромбоцитов и эритроцитов, выполняет функцию депо крови.
Классификация
В абдоминальной хирургии выделяют следующие виды разрывов селезенки:
- Контузия – наблюдается разрыв участка паренхимы при сохранении целостности капсулы органа.
- Разрыв капсулы без значительного повреждения паренхимы.
- Одномоментный разрыв селезенки – одномоментное повреждение капсулы и паренхимы.
- Двухмоментный разрыв селезенки – разрыв паренхимы, за которым через некоторое время следует разрыв капсулы.
- Разрыв капсулы и паренхимы с самостоятельной тампонадой (мнимый двухмоментный разрыв) – разрыв паренхимы быстро «закрывается» сгустком крови и кровотечение прекращается еще до появления выраженной клинической симптоматики. В последующем сгусток вымывается током крови, кровотечение возобновляется.
- Мнимый трехмоментный разрыв – двухмоментный разрыв, за которым через некоторое время следует самостоятельная тампонада, а позже – свободное позднее кровотечение.
Чаще всего наблюдаются одномоментные разрывы селезенки с немедленным возникновением кровотечения в брюшную полость. Двухмоментные разрывы составляют около 13% от общего количества закрытых повреждений селезенки, временной период между моментом травмы и началом кровотечения в брюшную полость колеблется от нескольких часов до 1-2,5 недель. Причиной разрыва капсулы при уже имеющейся центральной или подкапсульной гематоме становится физическое напряжение, чихание, кашель, ходьба, акт дефекации, поворот в постели и другие обстоятельства, вызывающие повышение давления в селезенке.
Большинство разрывов селезенки небольшие, сопровождаются стертой симптоматикой и диагностируются лишь через несколько часов, когда состояние больного ухудшается из-за продолжающейся кровопотери и скопления достаточного количества крови в брюшной полости. Профузное кровотечение с резким нарастанием клинических симптомов чаще наблюдается при двухмоментных повреждениях селезенки.

Симптомы разрыва селезенки
Клиника повреждений селезенки отличается большим разнообразием. Выраженность и наличие тех или иных проявлений зависят от степени разрыва, наличия или отсутствия сопутствующих повреждений, а также времени с момента травмы. Сразу после травматического воздействия может наблюдаться либо нерезкое ухудшение состояния, либо картина острой кровопотери без перитонеальных признаков, свидетельствующих о повреждении паренхиматозного органа. Основными жалобами в первые часы являются боли в районе левого подреберья и верхних отделах живота. Примерно у половины пациентов боли иррадиируют в левую лопатку и левое плечо.
Большинство больных принимают вынужденную позу: на левом боку с поджатыми ногами либо на спине. Брюшная стенка не участвует в акте дыхания. Степень напряжения брюшной стенки и выраженность болевого синдрома при пальпации живота может значительно варьировать как у разных больных, так и у одного и того же пациента в разные периоды после травмы. В отдельных случаях (при коллапсе или шоке) напряжение мышц живота может отсутствовать. Притупление звука в отлогих отделах живота при перкуссии наблюдается только при значительном кровотечении. Через некоторое время после травмы развивается парез кишечника, проявляющийся отсутствием дефекации, задержкой газов и вздутием живота.
Наряду с местными симптомами, наблюдается картина нарастающей острой кровопотери: бледность, липкий холодный пот, снижение АД, учащение пульса, рвота и тошнота, головокружение, прогрессирующая слабость, одышка и шум в ушах. В дальнейшем возможно двигательное возбуждение, сменяющееся потерей сознания, а также учащение пульса свыше 120 уд/мин и снижение АД ниже 70 мм рт. ст. При этом точно установить причину кровотечения на основании одних лишь клинических признаков удается не всегда, поскольку большинство перечисленных выше симптомов (за исключением болей в левом подреберье) непатогномоничны и появляются при любых острых катастрофах в животе.
Диагностика
Анализы крови на начальных этапах обследования малоинформативны, поскольку из-за механизмов компенсации кровопотери состав периферической крови может оставаться в пределах нормы в течение нескольких часов. Диагноз выставляется на основании клинических признаков, данных рентгенографии грудной клетки и рентгенографии живота. На рентгеновских снимках слева под диафрагмой определяется гомогенная тень. Дополнительными признаками разрыва являются ограничение подвижности и высокое стояние левого купола диафрагмы, расширение желудка, смещение левой части ободочной кишки и желудка вправо и книзу. При скудной клинической симптоматике, подкапсульных и центральных гематомах селезенки данные рентгенографии часто неспецифичны. Может потребоваться ангиография, однако этот метод не всегда применим из-за больших временных затрат, отсутствия необходимого оборудования или специалистов.
В настоящее время в связи с широким распространением эндоскопических методов все большее значение в диагностике разрывов селезенки приобретает лапароскопия. Эта методика позволяет не только быстро подтвердить наличие кровотечения в брюшную полость, но и точно установить его источник. При отсутствии эндоскопического оборудования альтернативой лапароскопии может стать лапароцентез – метод, при котором переднюю брюшную стенку прокалывают троакаром (полым инструментом), затем вводят через троакар катетер и выполняют аспирацию содержимого брюшной полости. Данная методика дает возможность подтвердить наличие кровотечения в брюшную полость, но не позволяет установить его источник.
Лечение разрыва селезенки
Кровотечения при подобных повреждениях крайне редко останавливаются самостоятельно, поэтому такая травма является показанием для экстренного хирургического вмешательства. Операция должна быть проведена в как можно более ранние сроки, поскольку нарастающая кровопотеря ухудшает прогноз. При возможности перед началом вмешательства добиваются стабилизации гемодинамики, осуществляя переливание крови и кровезаменителей. Если гемодинамические показатели не удается стабилизировать, операцию проводят даже при тяжелом состоянии пациента, параллельно продолжая осуществлять активные реанимационные мероприятия.
Классическим общепризнанным в травматологии и абдоминальной хирургии способом остановки кровотечения при любых разрывах селезенки считается полное удаление органа. Однако в последние годы, наряду с полным удалением, при отрывах фрагментов и неглубоких одиночных повреждениях некоторые хирурги в качестве варианта рассматривают органосохраняющую операцию – ушивание ран селезенки. Безусловными показаниями к полному удалению органа являются обширные разрывы и размозжения, разрывы в области ворот, обширные рваные и сквозные раны, невозможность надежного ушивания раны и прорезывание швов. В послеоперационном периоде после ушивания или удаления селезенки продолжают внутривенные инфузии крови и кровезаменителей, проводят коррекцию нарушений деятельности различных органов и систем, назначают обезболивающие и антибиотики.
Автор статьи

Читайте также:
- Иностранные государства и международные организации как субъекты природоресурсного права
- Кто может обратиться в конституционный суд рф с запросом о толковании конституции рф
- Средства расходной части государственного бюджета тратятся на уплату налогов
- Расписка как доказательство оплаты услуг представителя в суде
- Срок подачи протокола в суд

